芯空一号快讯 | 吸烟如何让牙周炎失控?高分辨率空间转录组揭示关键病理环路

文章背景
长期吸烟不仅是牙周炎的高危因素,更会以我们肉眼难以察觉的方式逐步侵蚀牙龈组织。本研究基于Visium HD空间转录组,对吸烟相关牙周炎(SP)患者的牙龈组织进行系统解析,构建了横跨上皮-基质-血管--免疫的空间病理网络。研究不仅描绘了细胞组成与结构的改变,还揭示了血管内皮与巨噬细胞的异常串扰是炎症升级的关键驱动,为吸烟诱导牙周组织破坏提供了关键机制证据,并指向潜在的靶点干预方向。
研究设计
本研究采用Visium HD空间转录组技术,在FFPE牙龈组织上实现2×2μm级亚细胞分辨率的转录组捕获。研究共纳入12例受试者,包括健康对照(HC,n=4)、慢性牙周炎(P,n=4)与吸烟相关牙周炎(SP,n=4)。
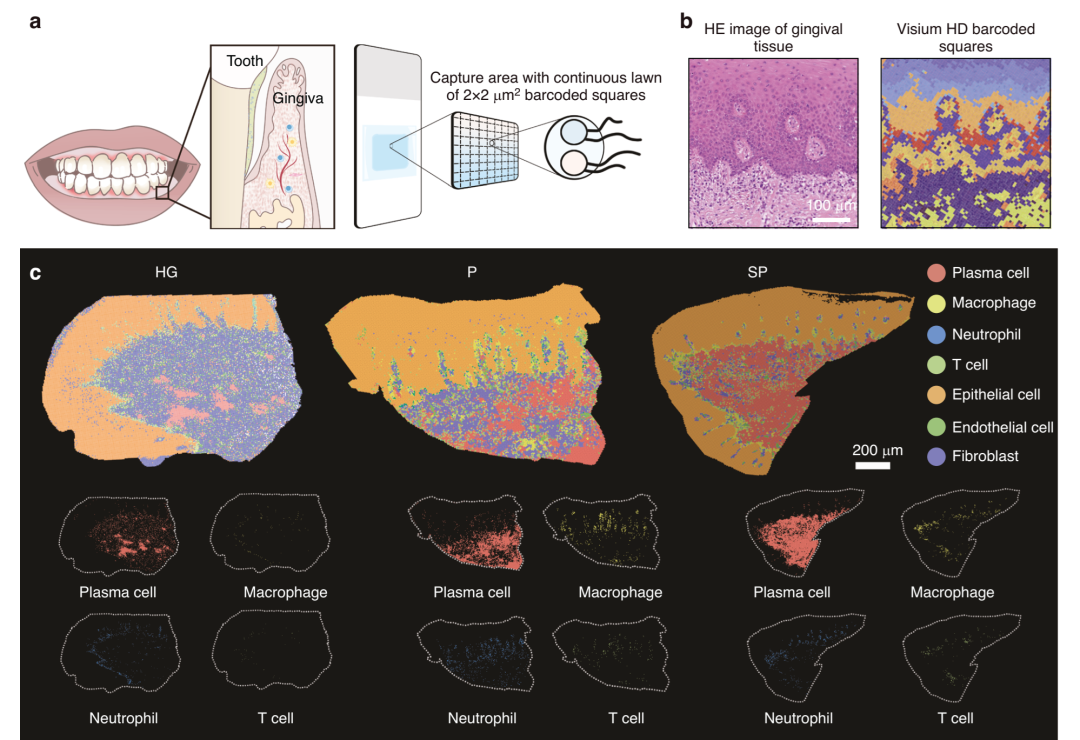
研究设计
文章结论
1.吸烟直接破坏牙龈上皮的屏障结构,使其从保护层转变为病变易感层
Visium HD空间转录组显示,在吸烟相关牙周炎(SP)中,上皮细胞的角化与损伤相关基因KRT1、KRT5、DSG1、PI3显著上调,而GPX2等抗氧化与保护因子下调,提示氧化压力与损伤修复失衡。受损信号呈沿牙龈黏膜表层带状分布,对应最易暴露于烟草刺激的区域。这一阶段上皮呈现高增殖–低稳态表型,细胞连接与屏障功能下降,使牙周局部对菌斑与免疫刺激更加敏感,成为后续病理级联的起点。
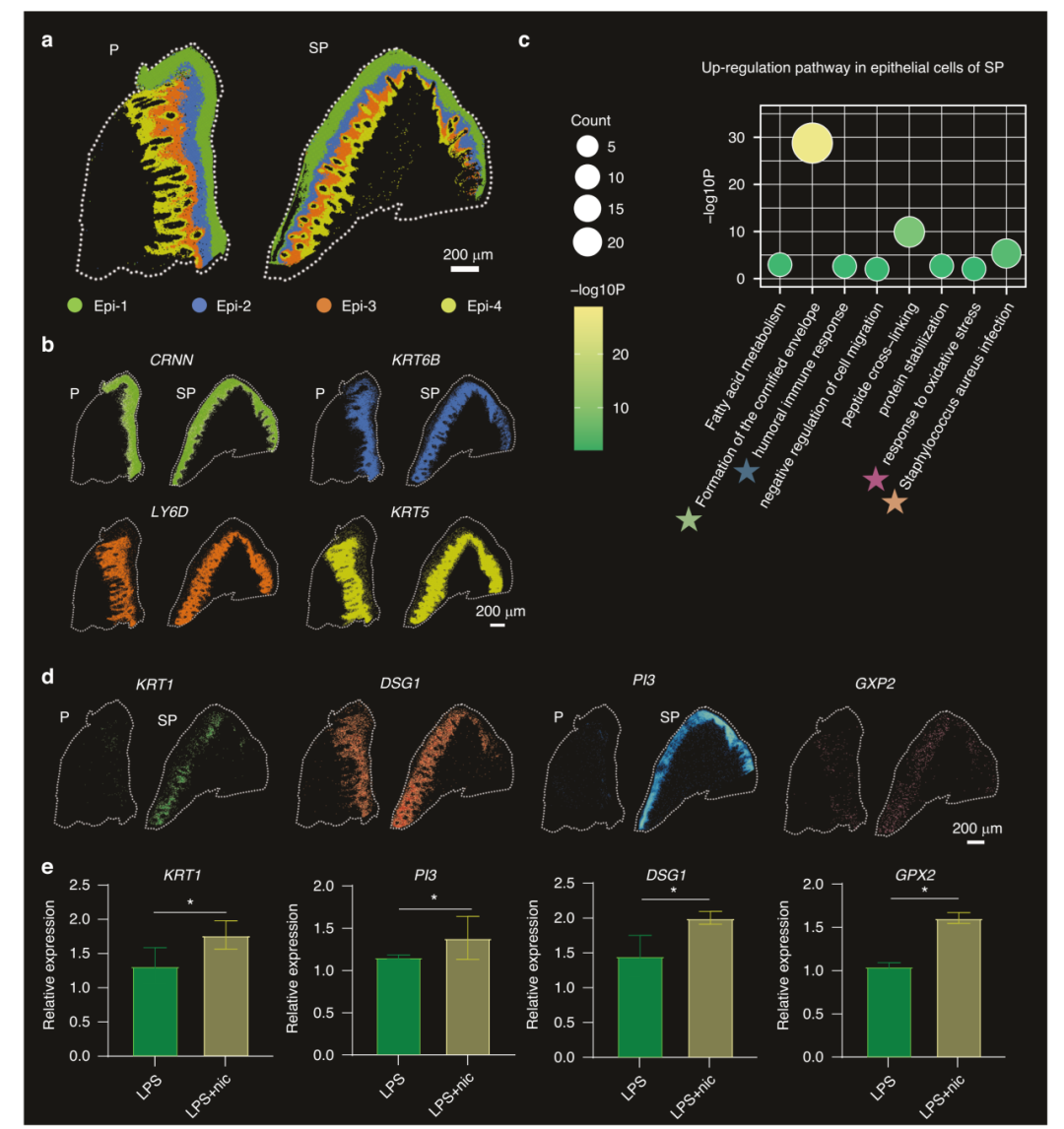
吸烟引起的牙龈上皮细胞损伤
2.成纤维细胞在吸烟微环境中产生病理性重塑反应,其修复机制由原本的维护支持转向炎症驱动与结构破坏
在SP中,成纤维细胞亚群构成发生明显偏移,其中伴随衰老、趋化与伤口修复信号异常增强的Fib-8亚群显著扩增。这些细胞持续分泌促炎与重塑因子,并通过EPGN–EGFR、WNT5A–SFRP2、AGRN–PTPRS等信号强化与受损上皮的异常互作,打破原有的屏障平衡,形成损伤修复–炎症激活正反馈回路。空间共定位进一步表明,这类炎症型成纤维细胞大量聚集于上皮损伤带下方,使上皮损伤不再是局灶事件,而演变为连续播散的组织结构失衡。
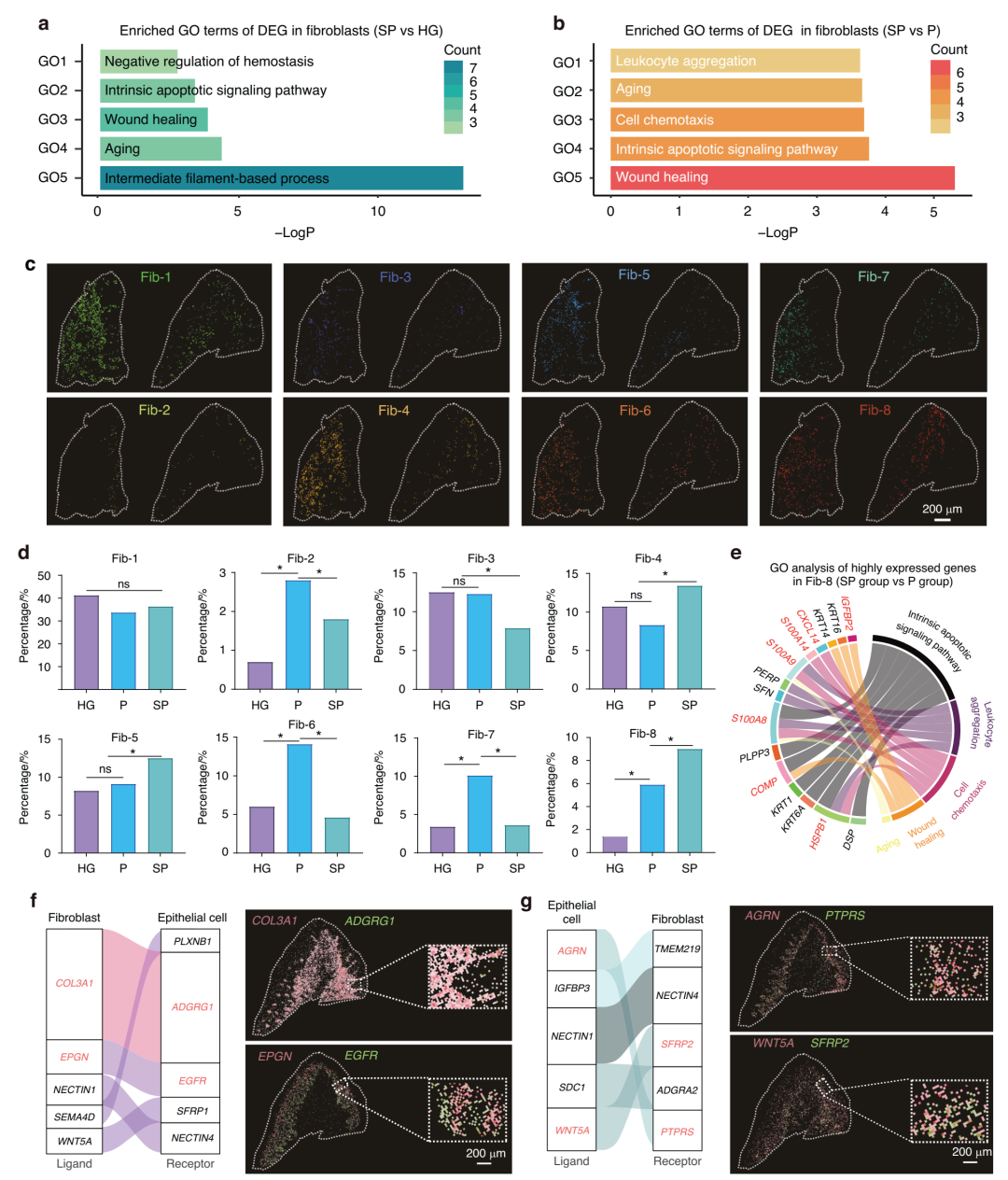
吸烟诱导的成纤维细胞改变和成纤维细胞与上皮细胞通讯的失调
3.CXCL12-CXCR4信号放大内皮-免疫互作,推动牙周炎进入不可逆阶段
SP患者中,内皮细胞呈现明显的压力与炎症响应表型,PECAM、NFKB1、STAT3、HIF1A等通路活跃,最突出的变化是CXCL12显著上调。CXCL12与巨噬细胞受体CXCR4空间高度共定位,使巨噬细胞向M1促炎方向极化,进一步增强局部炎症反应。
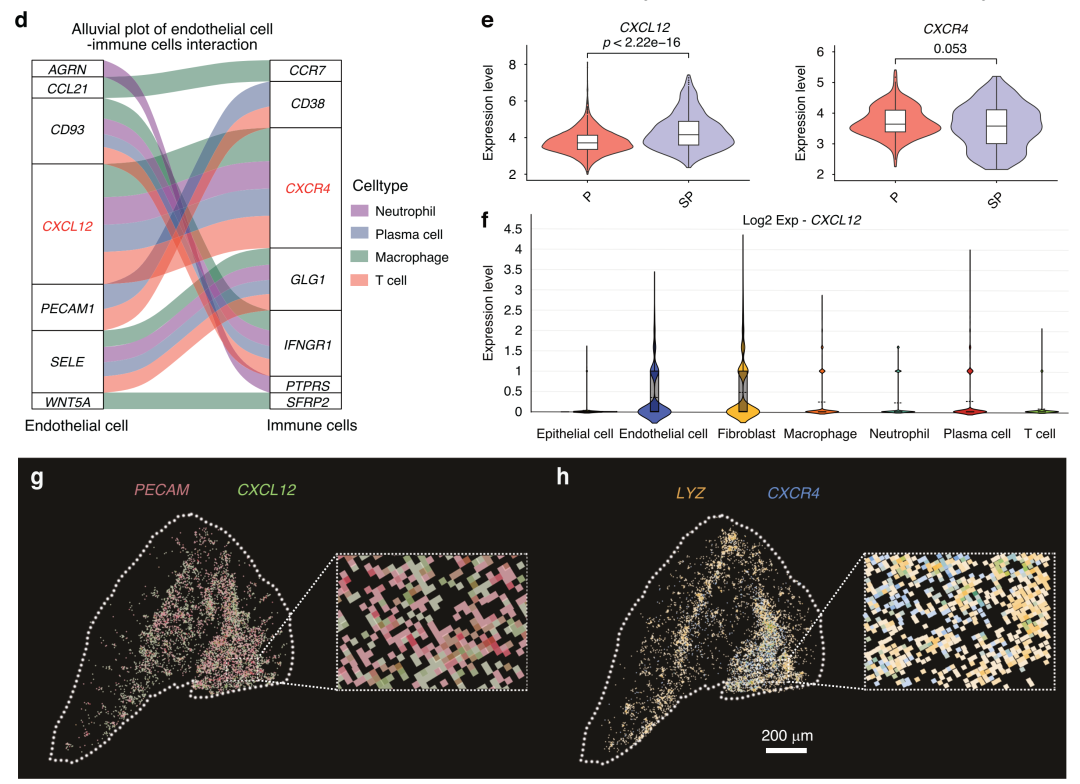
血管内皮CXCL12上调触发CXCR4免疫回路
动物实验(AAV-shCXCL12)证实,靶向抑制内皮CXCL12能够逆转巨噬细胞表型、降低炎症负荷并显著减轻牙槽骨吸收,提示内皮-免疫轴不仅是关键机制,更是可干预靶点,是吸烟导致牙周疾病从可逆炎症走向结构破坏的关键节点。
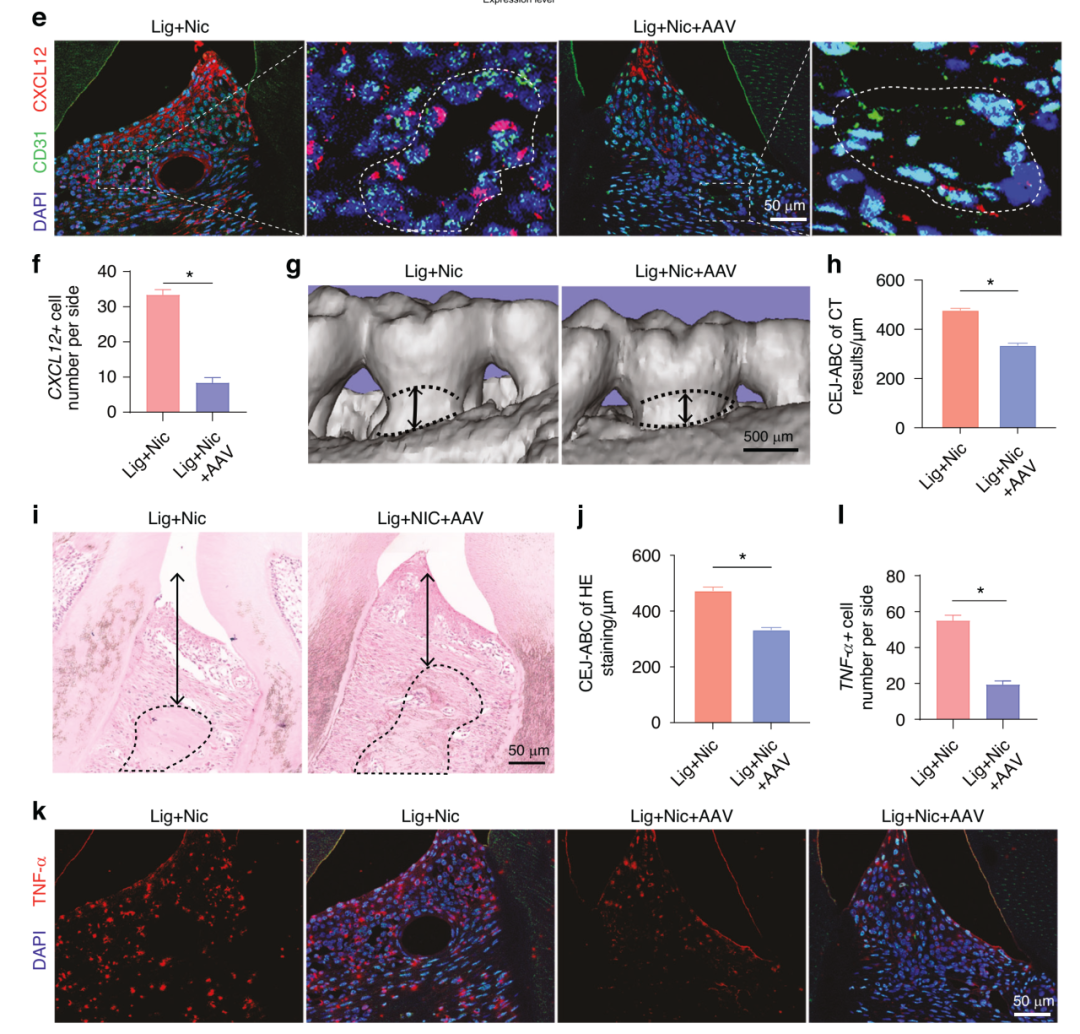
靶向内皮CXCL12可促进巨噬细胞极化至抗炎表型,从而减轻牙周炎症和骨吸收
文章总结
本研究在空间尺度上揭示了吸烟导致牙周炎加速进展的机制链条:上皮屏障破坏--成纤维细胞病理重塑--内皮免疫炎症回路形成,这一级联过程使牙龈组织失去原有的结构保护、修复自稳与炎症平衡能力,导致病程进入不可逆性破坏通道。尤其是CXCL12-CXCR4信号轴作为内皮-巨噬细胞间的病理通信枢纽,直接关联炎症传播与骨组织破坏,具备明确的干预与转化价值。
新闻中心
News Senter
上海生物芯片有限公司
Shanghai Biochip Co., Ltd.
版权所有©上海生物芯片有限公司
电子邮箱:
marketing@shbiochip.com
地址: 上海市浦东新区张江高科技园区李冰路151号
技术电话:
4001002131
扫描查看
微信公众号

